Головоломки
Химические опыты
Фараоновы змеи
Фараоновыми змеями называют целый ряд реакций, которые сопровождаются образованием пористого продукта из небольшого объема реагирующих веществ. Эти реакции сопровождаются бурным выделением газа. В итоге выглядит реакция так, будто из смеси реагентов выползает большая змея и ползет по столу, как настоящая.
На этой страничке вы узнаете про реакции, сопровождающиеся образованием "фараоновых змей", познакомитесь с уравнениями этих реакций и сможете посмотреть впечатляющие видеоролики, демонстрирующее ход таких реакций. Часть из этих реакций можно воспроизвести даже в домашних условиях или в школьной лаборатории - с соблюдением всех правил безопасности, разумеется. А другая часть реакций, к счастью, требует наличия таких реагентов, которых вы нигде, кроме как в специализированных лабораториях, не найдете. К счастью - потому что многие из них высокотоксичны, и экспериментировать с ними категорически не рекомендуется.
1. Разложение роданида (тиоцианата) ртути - Hg (CNS)2
Термическое разложение роданида ртути идёт по уравнению:
2 Hg(SCN)2 = 2 HgS + CS2 + C3N4
CS2 + 3O2 = CO2 + 2SO2
При нагревании роданида ртути образуются черная соль - сульфид ртути, нитрид углерода желтого цвета и дисульфид углерода CS2. Последний на воздухе воспламеняется и сгорает, образуя диоксид углерода CO2 и диоксид серы SO2.
Нитрид углерода вспучивается образующимися газами, при движении он захватывает черный сульфид ртути (II), и получается желто-черная пористая масса.
В результате из кусочка роданида ртути вылезает большая "змея" черно-желтого цвета, похожая на ужа, а то и не одна. Голубое пламя, из которого выползает "змея" - это пламя горящего сероуглерода CS2. Из 1 г тиоцианата аммония и 2,5 г нитрата ртути в умелых руках может получиться змея длиной 20-30 см.

Разложение тиоцианата ртути - первая из открытых реакций этого типа. Ее первооткрыватель - студент Гейдельбергского университета Фридрих Вёлер (1800—1882). Как-то раз осенью 1820 года, смешивая водные растворы тиоцианата аммония NH4NCS и нитрата ртути Hg(NO3)2, он обнаружил, что из раствора выпадает белый осадок. Вёлер отфильтровал раствор и высушил осадок полученного тиоцианата ртути Hg(NCS)2. Из любопытства исследователь поджег его. Осадок загорелся и произошло чудо: из невзрачного белого комочка, извиваясь, выползла и стала расти длинная черно-желтая "змея".
Cоли ртути ядовиты, и работа с ними требует осторожности и внимания. Безопаснее показывать змею дихроматную.
2. Дихроматная змея
Способ 1. Смешивают 10 г дихромата калия K2Cr2O7, 5 г нитрата калия KNO3 и 10 г сахара (сахарозы) C12H22O11. Затем растирают смесь в ступке и увлажняют этиловым спиртом C2H5OH или коллодием (он продается в аптеке). Затем эту смесь спрессовывают в стеклянной трубочке диаметром 5–8 мм.
Полученный столбик выталкивают из трубочки и поджигают с одного конца. Вспыхивает едва заметный огонек, из-под которого начинает выползать сначала черная, а потом зеленая «змея». Столбик смеси диаметром 4 мм горит со скоростью 2 мм в секунду. При горении он может удлиниться в 10 раз!

Реакция горения сахарозы в присутствии двух окислителей – нитрата калия и дихромата калия – довольно сложна. Продукты реакции - черные частицы сажи, зеленый оксид хрома (III) Cr2O3, расплав карбоната калия K2CO3, диоксид углерода CO2 и нитрит калия KNO2. Углекислый газ CO2 вспучивает смесь твердых продуктов и заставляет ее двигаться.
Способ 2. Смешать 1 г дихромата аммония (NH4)2Cr2O7 2 г нитрата аммония NH4NO3 и 1 г сахарной пудры. Смочить смесь водой, вылепить из нее палочку и высушить на воздухе. Если палочку поджечь, из нее в разные стороны поползут черно-зеленые «змеи».
При поджигании смеси происходят следующие реакции:
(NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O,
NH4NO3 = N2O + 2H2O,
C12H22O11 + 6O2 = 6CO2 + 11H2O + 6C.
При разложении дихромата аммония образуются азот N2, водяной пар и зеленый оксид хрома (III) Cr2O3. Реакция протекает с выделением теплоты. В реакции термического разложения нитрата аммония выделяется бесцветный газ – оксид диазота N2O, который уже при слабом нагревании разлагается на кислород O2 и азот N2. Горение сахара дает еще один газ – диоксид углерода CO2 , вдобавок происходит обугливание – выделение углерода. Большой объем газов плюс твердые продукты окисления – вот секрет «змеиного» поведения смеси.
3. Гадюка из соды и сахара
Для проведения этого опыта в столовую тарелку насыпают 3–4 ложки сухого просеянного речного песка и делают из него горку с углублением в вершине. Затем готовят смесь, состоящую из 1 чайной ложки сахарной пудры и 1/4 чайной ложки гидрокарбоната натрия NaHCO3 (питьевая сода). Песок пропитывают 96–98%-м раствором этанола C2H5OH и насыпают в углубление горки приготовленную реакционную смесь. Затем поджигают горку.
Спирт загорается. Через 3–4 минуты на поверхности смеси появляются черные шарики, а у основания горки – черная жидкость. Когда почти весь спирт сгорит, смесь чернеет, и из песка медленно выползает извивающаяся толстая черная «гадюка». У основания она окружена «воротником» догорающего спирта.

В этой массе происходят следующие реакции:
2NaHCO3 = Na2CO3 + H2O + CO2,
C2H5OH + 3O2 = 2CO2 + 3H2O
Диоксид углерода CO2, выделяющийся при разложении гидрокарбоната натрия и горении этилового спирта, а также водяные пары вспучивают горящую массу, заставляя ее ползти, как змея. Чем дольше горит спирт, тем длиннее получается «змея». Она состоит из карбоната натрия Na2CO3, смешанного с мельчайшими частичками угля, образованного при горении сахара.
4. Нитратный червяк
Вместо гидрокарбоната натрия можно использовать нитрат аммония NH4NO3. В столовую тарелку насыпают 3-4 ложки просеянного речного песка, делают из него горку с углублением в вершине и готовят реакционную смесь, состоящую из 1/2 чайной ложки нитрата аммония и 1/2 чайной ложки сахарной пудры, тщательно перетертых в ступке. Затем в углубление горки наливают 1/2 столовой ложки этилового спирта и насыпают 1 чайную ложку приготовленной нитратно-сахарной смеси. Теперь, если поджечь спирт, на поверхности смеси сразу же появляются черные шарики обугленного сахарного песка, и вслед за ними вырастает черный блестящий и толстый "червяк". Если нитратно-сахарной смеси было взято не более 1 чайной ложки, то длина червяка не превысит 3-4 см. А его толщина зависит от диаметра углубления горки.

Появление червяка вызвано взаимодействием нитрата аммония с сахаром, которое выражается следующим уравнением:
2NH4NO3 + C12H22O11 = 11C + 2N2 + CO2 + 15H2O.
"Червя" приводят в движение газы: азот N2, диоксид углерода CO2 и пары воды.
5. «Черный удав» из стакана
Этот опыт представляет собой впечатляющее зрелище. Сахарную пудру в количестве 75 г помещают в высокий стеклянный стакан, смачивают ее 5–7 мл воды и перемешивают длинной стеклянной палочкой. Потом к влажному сахару приливают по этой палочке 30–40 мл концентрированной серной кислоты H2SO4. Затем смесь быстро перемешивают стеклянной палочкой и оставляют в стакане.
Через 1–2 минуты содержимое стакана начинает чернеть, вспучиваться и в виде объемистой, рыхлой и ноздреватой массы подниматься, увлекая вверх стеклянную палочку. Смесь в стакане сильно разогревается, даже немного дымится, - и медленно выползает из стакана.

Серная кислота отнимает от сахара (сахароза C12H22O11) воду, разрушая его молекулярную структуру, и окисляет его, превращаясь при этом в диоксид серы SO2. При окислении сахара получается диоксид углерода CO2. Эти газы вспучивают образующийся уголь и выталкивают его из стакана вместе с палочкой.
Уравнение, передающее эти химические превращения, выглядит так:
C12H22O11 + 2H2SO4 = 11C + 2SO2 + CO2 + 13H2O.
Диоксиды углерода и серы вместе с парами воды увеличивают объем реакционной массы и заставляют ее подниматься вверх в узком стакане.
6. Уротропиновая змея
Для проведения этого опыта вам следует запастись терпением, но оно того стоит!
Для опыта понадобится уротропин (гексаметилентетрамин - (CH2)6N4). Таблетки уротропина можно купить в аптеке - это антисептический препарат. Подойдет также “твердый спирт” (сухое горючее) — его можно приобрести в хозяйственном магазине. Только убедитесь что сухое горючее, которое вы покупаете, содержит уротропин - оно бывает разных видов. Чтобы убедиться, что сухое горючее содержит уротропин, проведите простой опыт. Отломите несколько кусочков сухого горючего, положите их в пробирку и немного нагрейте. Если оно состоит из уротропина, вы почувствуете запах аммиака.
Чтобы сделать "змею", нужно произвести следующие действия. Одну таблетку “твердого спирта” или аптечного уротропина положите на блюдце и 3-4 раза пропитайте концентрированным водным раствором нитрата аммония NH4NO3, капая его из пипетки, а потом высушивая. Каждый раз надо наносить по 5-10 капель (0,5 мл раствора).
Высушивание таблеток - самая утомительная часть опыта: при комнатной температуре на воздухе оно продолжается слишком долго. Но повышать температуру для ускорения процесса нельзя - уротропин разлагается при высокой температуре. Тем более нельзя сушить таблетки на открытом огне: они могут загореться.
Пропитанную и высушенную таблетку на блюдце следует поджечь с одной стороны. И тут начнутся чудеса: появятся черные шарики кипящей жидкости, которые сливаются вместе и образуют подобие вырастающего “хвоста”. Он изгибается, а за ним из огня вырастает толстое тело “змеи”. “Змея” растет, упирается хвостом в блюдце, начинает изгибаться.

Разложение уротропина (CH2)6N4 в смеси с нитратом аммония NH4NO3 приводит к образованию пористой массы, состоящей из углерода, и большого количества газов - диоксида углерода СО2, азота N2 и воды:
(CH2)6N4 + 2NH4NO3 + 7О2 = 10C + 6N2 + 2CO2 + 16H2O
Интересно, что если смешать химически чистый уротропин и нитрат аммония, то разлагаются, не образуя твердых продуктов. Но в таблетки на стадии их формования добавляют связующие вещества - парафин и тальк. Вот почему появляется “тело змеи”. А выделяющиеся газы вспучивают и двигают его.
7. Глюконатная змея
Это самый простой и безопасный способ получения глюконатной змеи - для этого достаточно поднести к пламени таблетку глюконата кальция, который продается в каждой аптеке. Можно положить таблетку глюканата кальция на таблетку сухого спирта и поджечь его. Из таблетки выползет светло-серая "змея" с белыми пятнами, объем которой намного превышает объем исходного вещества - она может достигнуть длины 10-15 см.

Разложение глюконата кальция, имеющего состав Са[CH2OH(CHOH)4COO]2 · H2O приводит к образованию оксида кальция, углерода, углекислого газа и воды.
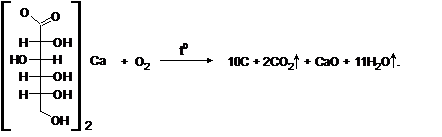
Светлый оттенок «змее» придает оксид кальция.
Недостатком образующейся «змеи» является ее хрупкость - она достаточно легко рассыпается.
8. Фараонова змея из сульфаниламида
Очень простой способ получения «фараоновых змей» – это окислительное разложение сульфаниламидных лекарственных препаратов (к ним относятся, например, стрептоцид, сульгин, сульфадиметоксин, этазол, сульфадимезин, фталазол, бисептол). В ходе окисления сульфаниламидных препаратов выделяется много газообразных продуктов реакции ( SO2, H2S , N2, пары воды), которые вспучивают массу и формируют пористую «змею».
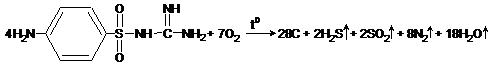
Опыт проводят только под тягой!
На таблетку сухого горючего помещают 1 таблетку лекарственного препарата и поджигают горючее. При этом происходит выделение блестящей «фараоновой змеи» серого цвета.

По своей структуре «змея» напоминает кукурузные палочки. Если выделяющуюся «змею» аккуратно подцепить пинцетом и осторожно вытягивать, то можно получить достаточно длинный «экземпляр».
9. Разложение нитроацетанилида
Для опыта понадобятся: фарфоровый тигель, треугольник, штатив, горелка, стеклянная палочка, шпатель. Соблюдать правила работы с концентрированной серной кислотой. При выполнении опыта не наклоняться над тиглем. Опыт выполняется под тягой.
Смешаем в фарфоровом тигле органическое вещество белого цвета - нитроацетанилид и серную кислоту. Нагреем смесь. Через несколько секунд из тигля выстрелит масса черного цвета. Выделяющиеся газы делают массу очень пористой и рыхлой.

Черный цвет массе придает углерод, образующийся в больших количествах. В еще больших количествах в ходе реакции образуются газы SO2, NO2 и CO2, которые вспенивают углерод.
Кстати...
А почему "фараоновы змеи"? Змеи - понятно, но почему фараоновы? В литературе можно найти следующее объяснение: "В одном из библейских преданий говорится, как пророк Моисей, исчерпав все иные аргументы в споре с фараоном, совершил чудо, превратив жезл в извивающуюся змею... Фараон был посрамлен и напуган, Моисей получил разрешение покинуть Египет, а мир получил очередную загадку". Звучит исчерпывающе, но только есть загвоздка: согласно Библии (книга "Исход"), пророк Моисей убедил фараона отпустить из рабства евреев, использовав куда мощные аргументы; их назвали "Десять казней египетских". Это были разные беды, которые Господь насылал на Египет после очередного отказа фараона отпустить еврейский народ. Ни одна из них, к слову, никак не была связана со змеями. Часть из этих ужасных чудес действительно сопровождались взмахами знаменитым жезлом. А знаменит он тем, что ему действительно приходилось побыть змеей, но сотворил это чудо вовсе не Моисей, а сам Господь, когда возлагал на него великую миссию, а Моисей стал проявлять малодушие.
Таким образом, остается непонятным, почему химических змей назвали "фараоновыми". Возможно, лишь потому, что такое название звучит солидно - под стать эффектности этого типа реакций.
Понравилось? Оставьте отзыв об этом материале!
-
Быстрый переход:
- Английский для детей
- Афоризмы
- Басни
- Былины
- Детские веснянки
- Высказывания
- Гадания
- Головоломки
- Гороскопы
- Детские дразнилки
- Загадки
- Заклички
- Игры
- Имена детей
- Мифы
- Небылицы
- Нумерология
- Переклички
- Детские песни
- Поговорки
- Подарки
- Поздравления для ребят
- Пословицы
- Потешки
- Прибаутки
- Приговорки
- Рассказы
- Детские сказки
- Скороговорки
- Сонники
- Статьи про детей
- Стихи
- Сценарии
- Считалки для ребят
- Фразеологизмы
- Фразы
- Цитаты
- Частушки
- Детский юмор

